BADANIA PHOSPHARE WYKAZAŁY ZNACZNIE NIŻSZĄ CZĘSTOŚĆ WYSTĘPOWANIA HIPOFOSFATEMII W PRZYPADKU STOSOWANIA DERIZOMALTOZY ŻELAZOWEJ W PORÓWNANIU Z KARBOKSYMALTOZĄ ŻELAZOWĄ1
PHOSPHARE-IDA
Dwa identyczne, randomizowane (1:1), otwarte badania porównawcze przeprowadzone z udziałem 245 pacjentów z niedokrwistością z niedoboru żelaza (IDA) oraz nietolerancją lub brakiem odpowiedzi na doustne preparaty żelaza. Derizomaltozę żelazową (FDI) podawano w pojedynczej dawce 1000 mg w postacie wlewu dożylnego przez 20 minut w dniu 0. Karboksymaltozę żelazową (FCM) podawano w dawce 750 mg w dniu 0 oraz 750 mg w dniu 7. Pełny opis projektu badania znajduje się poniżej.
Łączna częstość występowania hipofosfatemii (<2,0 mg/dl) w badaniach PHOSPHARE (pierwszorzędowy punkt końcowy)1
Procent pacjentów z hipofosfatemią od początku badania do 35. dnia:
- Badanie A: 7,9% po zastosowaniu FDI vs 75,0% po zastosowaniu FCM [skorygowana różnica częstości: –67,0% (95% CI: –77,4%, –51,5%)]
- Badanie B: 8,1% po zastosowaniu FDI vs 73,7% po zastosowaniu FCM [skorygowana różnica częstości: –65,8% (95% CI: –76,6%, –49,8%)]
- Dane łączone: 8,0% po zastosowaniu FDI vs 74,4% po zastosowaniu FCM [skorygowana różnica częstości: –68,3% (95% CI: –76,5%, –56,5%)]
Analiza post hoc: łączna częstość występowania ciężkiej hipofosfatemii (≤1,0 mg/dl)

Ograniczenia badania
W obu badaniach uczestniczyły głównie kobiety z niedokrwistością z niedoboru żelaza spowodowaną krwawieniem ginekologicznym, u których częstość występowania hipofosfatemii jest wyższa. To prawdopodobnie wyjaśnia wyższą niż oczekiwano częstość występowania hipofosfatemii po leczeniu karboksymaltozą żelazową. W badaniach nie mierzono wyników klinicznych.
Projekt badania – PHOSPHARE-IDA
Derizomaltoza żelazowa vs karboksymaltoza żelazowa – badanie przeprowadzone w 114 ośrodkach w USA1
Dwa identyczne, randomizowane, otwarte badania kliniczne z udziałem 245 pacjentów z niedokrwistością z niedoboru żelaza oraz nietolerancją lub brakiem skuteczności leczenia doustnymi preparatami żelaza.1
245 dorosłych pacjentów z niedokrwistością z niedoboru żelaza
Wybrane kryteria włączenia:
- ≥18 lat
- Hb ≤11 g/dl
- Stężenie ferrytyny <100 ng/ml
- Historia nietolerancji lub braku odpowiedzi na przyjmowanie doustnego preparatu żelaza przez co najmniej 1 miesiąc
Wybrane kryteria wyłączenia
- Pacjenci z obniżoną czynnością nerek
Wybrane dane demograficzne na początku badania:
- Badanie A: średni wiek, 45,1 lat; 95,9% kobiet
- Badanie B: średni wiek, 42,6 lat; 94,1% kobiet
Randomizacja 1:1
117 pacjentów w grupie otrzymującej karboksymaltozę żelazową
Badanie A: 60
Badanie B: 57
- 750 mg na dawkę w dniu 0 i w dniu 7
- 2 dawki (łącznie 1500 mg)
117 pacjentów w grupie otrzymującej derizomaltozę żelazową
Badanie A: 63
Badanie B: 62
- Pojedyncza dawka 1000 mg w dniu 0
- Infuzja ponad 20 minut
35-dniowy okres obserwacji
Pierwszorzędowy punkt końcowy1
Częstość występowania hipofosfatemii (poziom fosforanów w surowicy <2,0 mg/dl) między początkiem badania a dniem 35.
PHOSPHARE-IBD
BADANIE PORÓWNAWCZE Z UDZIAŁEM PACJENTÓW Z NIEDOKRWISTOŚCIĄ Z NIEDOBORU ŻELAZA I NIESWOISTYMI CHOROBAMI ZAPALNYMI JELIT2
To randomizowane, podwójnie zaślepione badanie kliniczne przeprowadzono w 20 ambulatoryjnych klinikach szpitalnych w Europie (Austria, Dania, Niemcy, Szwecja i Wielka Brytania). Dziewięćdziesięciu siedmiu dorosłych pacjentów z nieswoistymi chorobami zapalnymi jelit (IBD) oraz niedokrwistością z niedoboru żelaza (IDA) zostało losowo przydzielonych w stosunku 1:1 do otrzymania derizomaltozy żelazowej (n=49) lub karboksymaltozy żelazowej (FCM) (n=48) w dniu rozpoczęcia badania oraz w 35. dniu, zgodnie z identycznym schematem dawkowania opartym na stężeniu hemoglobiny i masie ciała.
Pacjenci w badaniu PHOSPHARE-IBD otrzymali 1000 mg FDI lub FCM w dniu 0. Następnie, w dniu 35., podano im 1000 mg lub 500 mg FDI albo odpowiednio 1000 mg lub 500 mg FCM — zgodnie z charakterystyką produktu leczniczego zatwierdzoną przez Europejską Agencję Leków dla obu preparatów.
Pierwszorzędowy punkt końcowy
- Częstość występowania hipofosfatemii (stężenie fosforanów w surowicy <2,0 mg/dl) od wartości początkowej do 35. dnia
Wybrane dodatkowe punkty końcowe
- Zmiana stężenia Hb od wartości początkowej do 70. dnia
- Zmiana wyniku w skali FACIT-Fatigue od wartości początkowej do 70. dnia
- Zmiana biomarkerów metabolizmu kości i minerałów od wartości początkowej do 70. dnia
- Częstość występowania zdarzeń niepożądanych i poważnych zdarzeń niepożądanych w dowolnym momencie badania
Częstość występowania hipofosfatemii była znacznie mniejsza w przypadku leczenia FDI w porównaniu z FCM od początkowego do 35. dnia (pierwszorzędowy punkt końcowy)2

ZMIANA STĘŻENIA HB, WYNIKI W SKALI FACIT-FATIGUE I STĘŻENIE FOSFORANÓW (DODATKOWE PUNKTY KOŃCOWE)2*
Zmiana stężenia Hb
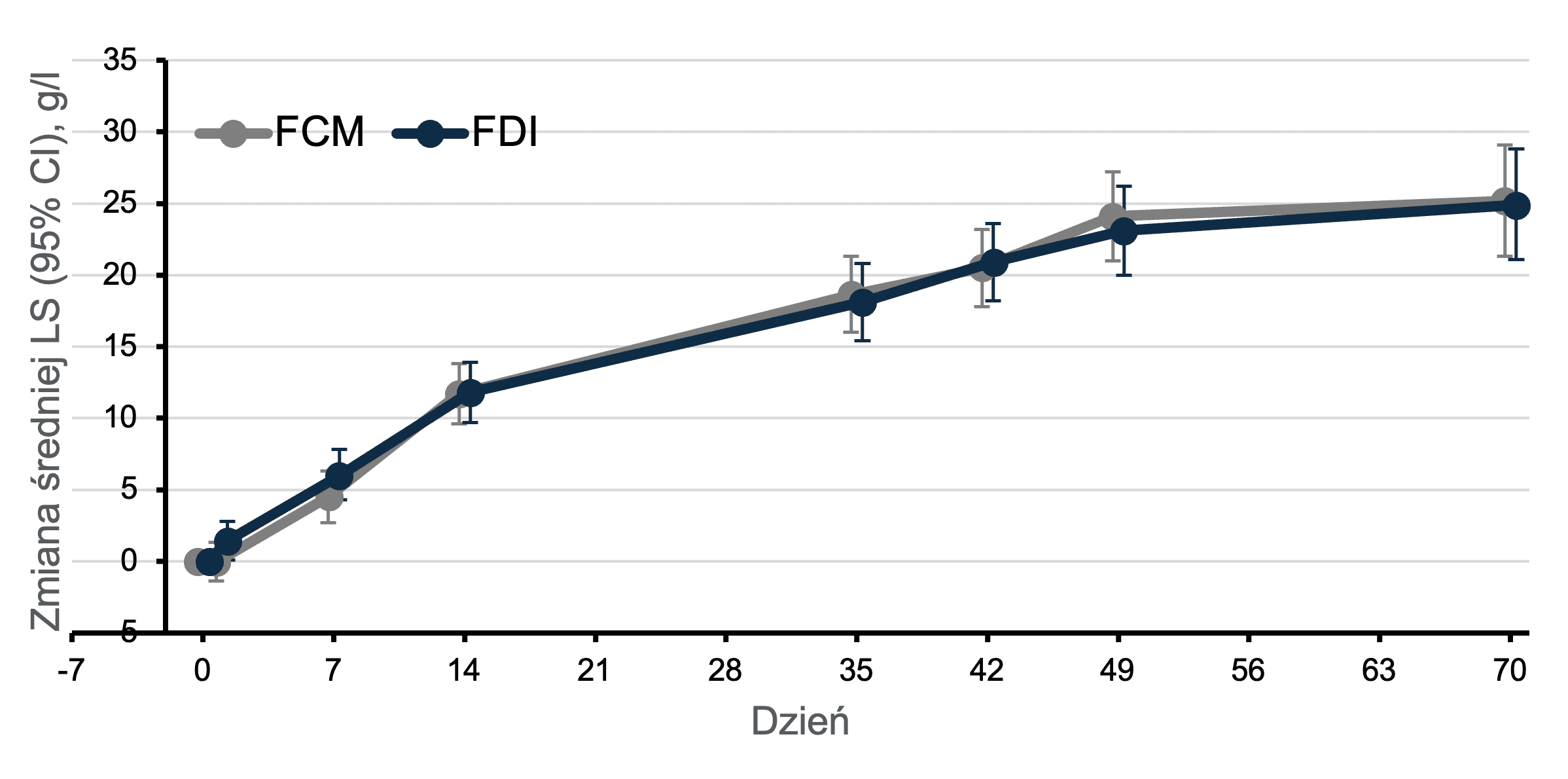
Zmiana wyniku w skali FACIT-Fatigue
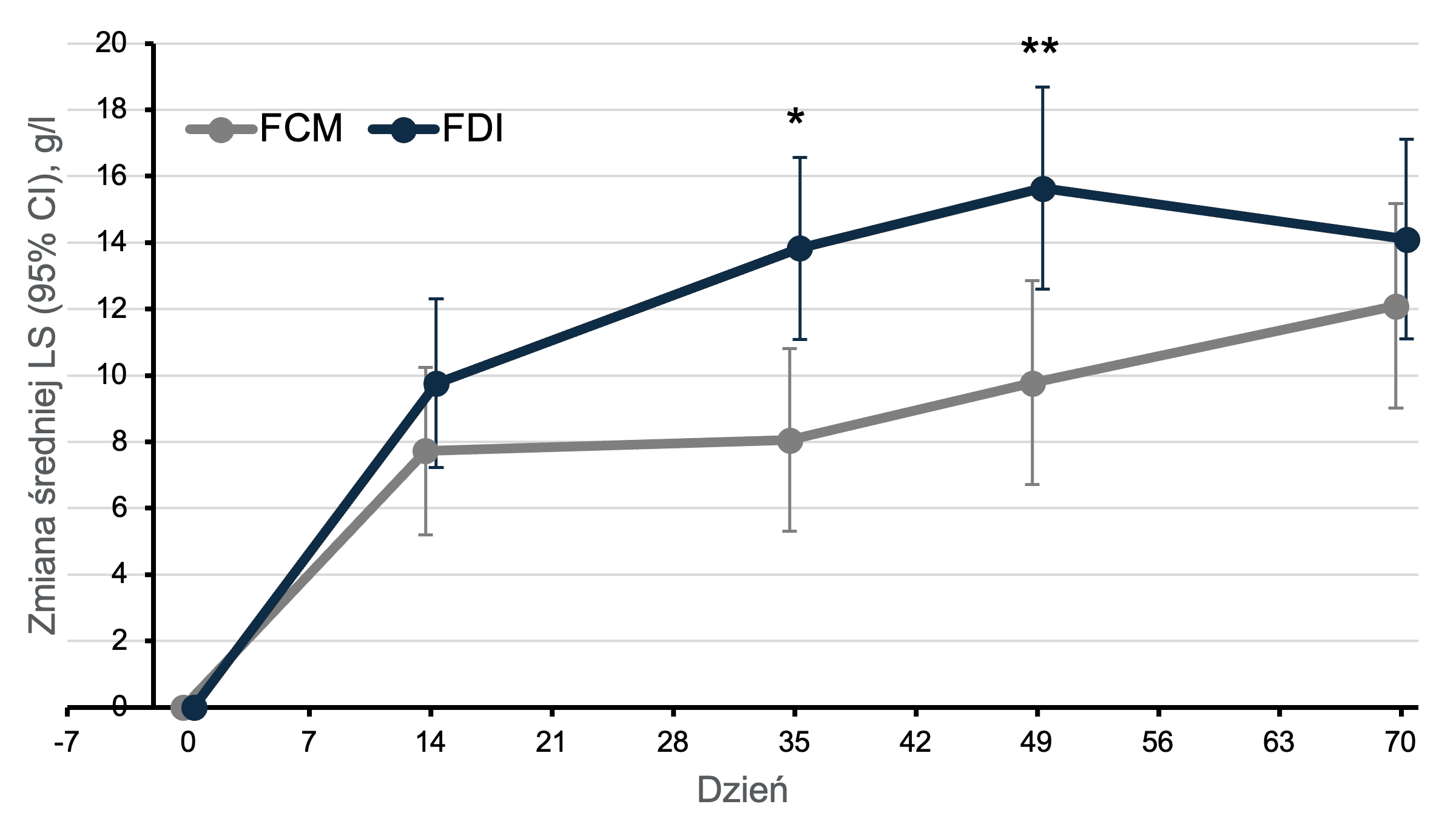
Zmiana w stężeniu fosforanów w surowicy
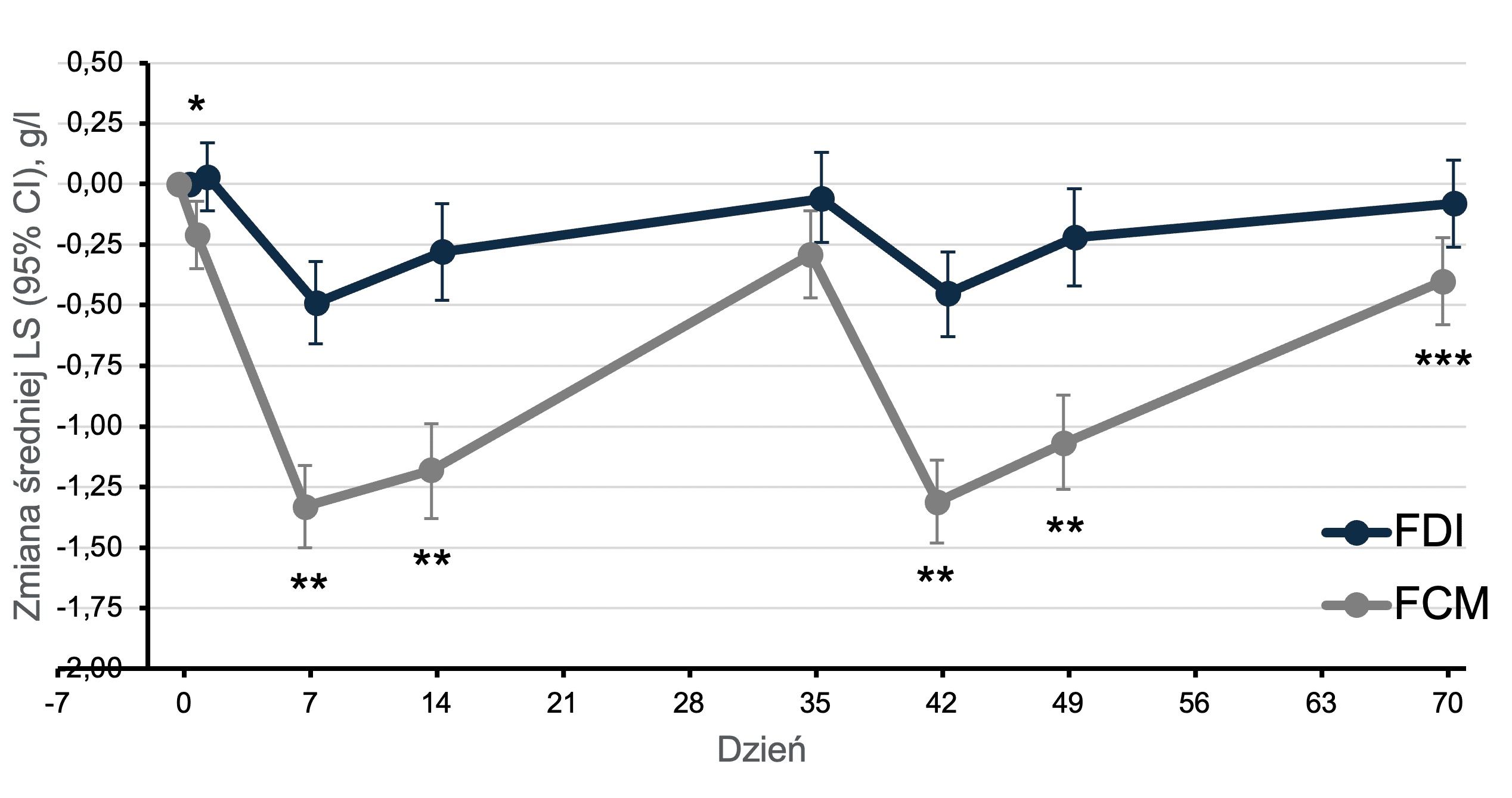
*Wykresy dotyczące zmiany stężenia Hb i FACIT-Fatigue oparto na populacji ITT, natomiast wykres dotyczący stężenia fosforanów wykorzystuje zestaw do analiz bezpieczeństwa.
Dane dotyczące bezpieczeństwa z badania PHOSPHARE-IBD
Zdarzenia niepożądane i poważne zdarzenia niepożądane występowały z porównywalną częstością w grupach przyjmujących FDI i FCM. Hipofosfatemia i niedobór witaminy D były zgłaszane częściej w grupie przyjmującej FCM niż w grupie przyjmującej FDI. Ból głowy i nudności były zgłaszane częściej w grupie przyjmującej FDI niż w grupie przyjmującej FCM.
Zdarzenia niepożądane
| FDI (n=48) | FCM (n=49) | |
| JAKIEKOLWIEK ZDARZENIA NIEPOŻĄDANE | 44 (91.7%) | 44 (89.8%) |
| NAJCZĘSTSZE ZDARZENIA NIEPOŻĄDANE (≥10% W CO NAJMNIEJ JEDNEJ GRUPIE LECZONEJ) | ||
| NIEDOBÓR WITAMINY D | 11 (22.9%) | 17 (34.7%) |
| HIPOFOSFATEMIA | 1 (2.1%) | 14 (28.6%) |
| NIEŻYT NOSA I GARDŁA | 8 (16.7%) | 10 (20.4%) |
| BÓL GŁOWY | 9 (18.8%) | 5 (10.2%) |
| BÓL STAWÓW | 7 (14.6%) | 6 (12.2%) |
| NUDNOŚCI | 6 (12.5%) | 1 (2.0%) |
| ZMĘCZENIE | 5 (10.4%) | 4 (8.2%) |
Szczegółowe informacje na temat badania można znaleźć w pełnej publikacji.
PHOSPHARE-IDA: https://pmc.ncbi.nlm.nih.gov/articles/PMC7042864/
PHOSPHARE-IBD: https://pmc.ncbi.nlm.nih.gov/articles/PMC10086283/
Referencje
- Wolf M, Rubin J, Achebe M, et al. Effects of Iron Isomaltoside vs Ferric Carboxymaltose on Hypophosphatemia in Iron-Deficiency Anemia: Two Randomized Clinical Trials. JAMA. 2020;323(5):432-443. doi:10.1001/jama.2019.22450
- Zoller H, Wolf M, Blumenstein I, et al. Hypophosphataemia following ferric derisomaltose and ferric carboxymaltose in patients with iron deficiency anaemia due to inflammatory bowel disease (PHOSPHARE-IBD): a randomised clinical trial. Gut. 2023;72(4):644-653. doi:10.1136/gutjnl-2022-327897


